| Indice | indietro | avanti |
La scoperta dell'elettrone

La data di nascita dell'elettrone è il 1897, anno in cui Joseph John Thomson (1865-1940), direttore del Cavendish Laboratory di Cambridge osservò che i raggi catodici erano sensibili ai campi elettrici e magnetici e che si comportavano come particelle cariche negativamente. Thomson progettò un esperimento per determinare le caratteristiche di queste particelle.
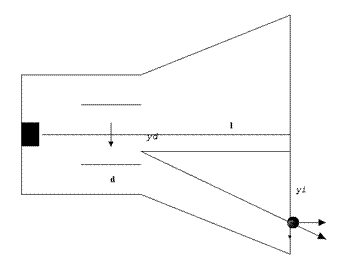
In un tubo a raggi catodici, le particelle negative (raggi catodici) sono emesse dal catodo e sparate a velocità elevata nel vuoto attraverso una zona d dove possono agire i campi elettrico e magnetico incrociati, perpendicolari rispetto alla velocità delle particelle. Dopo questo tratto il fascio, eventualmente deviato, attraversa una zona di deriva molto più lunga della precedente, fino a colpire una zona dello schermo fluorescente che si illumina nel punto colpito.
- Con i campi spenti il fascio non è deviato e colpisce la parte centrale dello schermo.
- Con un campo elettrico E (diretto verticalmente), il fascio è deviato verso l'alto o verso il basso. Si misura la deflessione verticale y che è funzione della geometria del sistema e delle caratteristiche della particella.
- Si regola quindi l'intensità del campo magnetico B finché la deflessione del fascio non viene annullata.
- Si misura in questo modo la velocità della particella v = E/B
Dalla misura della velocità, Thomson riuscì a determinare il rapporto carica/massa dei raggi catodici in funzione di altre grandezze dell'apparato: q/m =2 y E / B2 d2 (con y deflessione misurata con B=0). Il valore ottenuto sperimentalmente da Thomson fu: q/m = 1,76 1011 C/kg
Il valore trovato da Thomson risultava essere circa 2000 volte più grande di quello, conosciuto, del rapporto carica massa dello ione idrogeno (cioè del protone). Inoltre questo valore era sempre lo stesso indipendentemente dal materiale di cui era fatto il catodo. Thomson ipotizzò che queste particelle negative fossero una componente di tutti gli atomi. Non conoscendone né la massa, né la carica, erano possibili tre ipotesi:
- le particelle negative avevano la stessa massa dei protoni, ma carica 2000 volte maggiore
- le particelle negative avevano la stessa carica dei protoni, ma massa 2000 volte minore
- le particelle negative avevano sia la massa sia la carica diversa da quelle dei protoni

Modello atomico a panettone.
Thomson scelse la seconda ipotesi (che poi si rivelò giusta). Pensò anche (erroneamente) che la massa maggiore della parte positiva dell'atomo corrispondesse ad un volume maggiore ed immaginò un atomo in cui la parte positiva riempiva tutto il volume a disposizione, mentre le particelle negative (elettroni) erano piccole ed immerse nella massa positiva come l'uvetta nel panettone.
| Indice | indietro | avanti |
Copyleft Ludovica Battista