| Indice | indietro | avanti |
Polarizzazione dei dielettrici

All'interno di un condensatore può esserci semplicemente uno spazio vuoto oppure un mezzo costituito a sua volta da molecole: alcune molecole (dette apolari) sono dotate di una simmetria interna in modo tale che il centro delle cariche positive coincide con quello delle cariche negative.
Per altre molecole (come quella dell'acqua), dette polari, questo non avviene: i centri delle cariche positive e negative si trovano ad una certa distanza d. La molecola dell'acqua (H2O) è polare perché il centro della carica positiva è spostato verso gli atomi di idrogeno, mentre quello della carica negativa è spostato verso l'atomo di ossigeno.
Le molecole polari si comportano come microscopici dipoli elettrici caratterizzati dal valore assoluto della carica q e dalla distanza d tra le due cariche opposte.

Le dimensioni fisiche del momento di dipolo elettrico sono: [p] = [lunghezza corrente tempo] e la sua unità di misura nel SI è il C m (coulomb metro).
Spesso una molecola polare viene rappresentata schematicamente per mezzo del vettore p: si noti che p ha la punta rivolta verso la carica positiva, quindi ha verso contrario a quello del campo elettrico E di dipolo (le linee del campo elettrico creato dal dipolo vanno dalla carica positiva a quella negativa).
Una molecola d'acqua possiede un momento di dipolo elettrico di intensità p = 6,1 10-30 C m

- rimangono così come sono
- si spostano nella direzione del campo
- tendono ad allineare i momenti di dipolo nello stesso verso del campo
- tendono ad allineare i momenti di dipolo in verso opposto al campo
Il dipolo è sottoposto ad una coppia di forze (uguali e opposte). La forza risultante sul dipolo è pertanto nulla, ma non è nullo il momento meccanico (o momento torcente) e quindi la molecola è sottoposta ad una rotazione. La molecola ruota fin quando si annulla il momento meccanico, cioè quando si annulla il braccio della coppia.
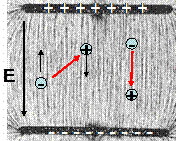
Le molecole polari immerse in un campo elettrico tendono quindi ad allinearsi alle linee di campo, con il momento di dipolo concorde con il verso del campo: si dice che il dielettrico subisce una polarizzazione per orientamento.
In realtà, a causa della agitazione termica disordinata, solo una piccola percentuale delle molecole riesce ad orientarsi.
- Il campo E non risente della presenza del mezzo
- Il campo E aumenta di intensità
- Il campo E diminuisce di intensità
Per capire cosa succede, dobbiamo pensare che ad ogni molecola polare corrisponde un microscopico campo elettrico rivolto in senso contrario al momento di dipolo. Tutte le molecole orientate sommano i loro campi elettrici, in modo da creare un campo elettrico E' contrario al campo E preesistente nel vuoto. Anche se la percentuale di molecole orientate non è alta a causa dell'agitazione termica, la loro disposizione ordinata riesce a far diminuire il campo elettrico preesistente.
Cosa accade in presenza di un mezzo non polare? Le molecole apolari hanno una simmetria spaziale e non posseggono un proprio momento di dipolo, ma il campo elettrico esterno provoca uno stiramento della molecola e quindi un successivo orientamento. Questo fenomeno si chiama polarizzazione per deformazione. Gli effetti di questo secondo tipo di polarizzazione sono meno forti del primo. In ogni caso possiamo affermare che la presenza di un mezzo isolante (o dielettrico) tende a indebolire il campo elettrico preesistente.
| Indice | indietro | avanti |
Copyleft Ludovica Battista